一、选择(选出下列各题中惟一正确的答案。1—11题每题2分,12—13题每题3分,共28分。不选、多选、错选不得分)
1.加热某种固体有气体产生,对于这一变化的分析正确的是………………………( )
A.是化学变化 B.可能是物理变化,也可能是化学变化
C.是物理变化 D.既不是物理变化,也不是化学变化
2.“低碳”是指在生产和生活中不排放或少排放二氧化碳气体。下列能源的使用最符合“低碳”理念的是………………………………………………………………………( )
A.煤 B.石油 C.天然气 D. 太阳能
3.下列一定属于纯净物的是……………………………………………………………( )
A.由同种分子构成的物质 B.由不同种分子构成的物质
C.由同种元素组成的物质 D.由不同种元素组成的物质
4.水是人们生活、生产各方面都离不开的重要物质。下列有关水的说法错误的是…( )
A.水是一种最常用的溶剂 B.用肥皂水鉴别硬水和软水
C.自然界的水都含有杂质 D.电解是一种净化水的方法
5.在化学反应前后,肯定不会变化的是………………………………………………( )
①原子的数目 ②分子的数目 ③元素的种类 ④物质的质量总和 ⑤物质的种类
⑥物质的体积 ⑦物质的状态
A.②④⑤ B.①③④ C.①③④⑥ D.①③⑦
6.森林失火时,灭火队员通常要砍伐一些树木,开辟“防火隔离带”,其主要目的是( )
A.隔离空气 B. 降低可燃物的温度
C.隔离可燃物 D. 降低可燃物的着火点
7.实验室制取氧气,既可采用分解过氧化氢的方法,也可采用分解氯酸钾的方法。这两种方法的共同点是…………………………………………………………………( )
A.反应都不需要加热 B.所需仪器相同
C.均可用二氧化锰作催化剂 D.都利用氧化物分解
8.下列氯化钠溶液,其溶质的质量分数不等于15%的是……………………………( )
A.100 g水中溶解15 g氯化钠 B.氯化钠与水按15:85的质量比形成的溶液
C.100 g 溶液中含15 g氯化钠 D.30 g氯化钠溶解于170 g水中所形成的溶液
9.下列实验操作能达到预期目的的是………………………………………………… ( )
①用托盘天平称取5.6 g氧化铜粉末 ②用10 mL水和10 mL酒精配制成20 mL酒精溶液
③将50 g溶质质量分数为10%的盐酸加热蒸发掉25 g水,得到溶质质量分数为20%的盐酸 ④用10 mL量筒量取8.2 mL水
A.①④ B.①②④ C.①③④ D.②③
10.下列各组气体中,仅用燃着的木条不能将它们区分出来的是……………………( )
A.氧气和空气 B.二氧化碳和氮气
C.甲烷和空气 D.一氧化碳和二氧化碳
11.下列实验方案中,设计不合理的是…………………………………………………( )
A.用二氧化锰区别水和过氧化氢溶液
B.用过滤的方法将浑浊的水变为澄清的水
C.用燃烧木炭的方法制备纯净的二氧化碳气体
D.用熟石灰鉴别氯化铵和氯化钾
12.推理是化学学习中常用的思维方法。下列推理正确的是…………………………( )
A.中和反应生成盐和水,所以生成盐和水的反应一定是中和反应
B.碱能跟某些非金属氧化物反应,所以碱溶液能吸收一氧化碳气体
C.酸能使紫色石蕊溶液变红,通入二氧化碳后的紫色石蕊溶液变红,所以二氧化碳是酸
D.碱性物质的溶液能使无色酚酞溶液变红,所以能使无色酚酞溶液变红的物质不一定是碱
13.下列物质长久盛放在敞口的容器中,会变质且质量变大的是……………………( )
①浓盐酸 ②浓硫酸 ③烧碱 ④纯碱 ⑤生石灰 ⑥食盐
A.①⑥ B.②③④⑤ C.②③④ D.③⑤
得分评卷人
二、填空(共14分)
14.(4分)用H、S、O、Na四种元素,按下列要求写出物质的化学式。
(1)相对分子质量最小的氧化物:? ;(2)用于金属表面除锈的酸: ? ;
(3)厨房清洁剂中含有的碱: ? ; (4)由三种元素组成的一种盐: ?。
15.(6分)试用你所学过的化学知识解释下列问题或现象。
(1)食品密封包装时填充氮气可以防腐,这是因为 ? 。
(2)煤矿矿井内严禁烟火,这是因为 ? 。
(3)在盛有水的铁锅里,铁锅与水面接触的一圈锈蚀最为严重,这是因为
? 。
16.(4分)2011年3月11日,日本发生9.0级大地震,引发海啸,福岛核电站遭到破坏,核反应堆内的物质在高温下发生一系列化学反应,产生的大量氢气因泄漏与空气混合发生爆炸,该爆炸反应的化学方程式是 ? 。爆炸导致放射性物质外泄,引发核危机。其中碘-131就是一种放射性元素的原子,其原子核内有53个质子,78个中子,则它的核外有 ?个电子,属于 ? 元素(填“金属”或“非金属”)。
得分评卷人
三、应用(共16分)
17.(10分)食醋、食盐和纯碱都是日常生活中常用的物质。食醋中通常含有3%~5%的乙酸,乙酸俗称醋酸,是一种无色液体。食盐和纯碱都是白色固体。
(1)在用食醋拌凉菜时,往往可以闻到醋香,这说明醋酸具有 ? 性。食醋不宜存放在含铁等金属的容器内,原因是 ? 。请写一个你熟悉的酸与金属反应的化学方程式 ? 。
(2)用食醋可以鉴别食盐和纯碱。请简要写出实验步骤和现象: ?
? 。
(3)纯碱的水溶液能使紫色石蕊溶液变蓝,说明其水溶液显 ? 性,而在酸、碱、盐三类化合物中,纯碱属于 类。纯碱还能与许多化合物反应,请写一个你知道的纯碱与碱反应的化学方程式 ? 。
18.(6分)某学校开展综合实践活动,组织学生考察学校附近化工厂的污水处理情况,了解到该化工厂排放的污水中含有盐酸,经检测,污水中HCl的质量分数为0.0073%,处理污水所用的原料是熟石灰。
(1)要中和1000 t污水中的HCl,至少需要熟石灰的质量是多少?
(2)中和反应在生产生活中有广泛的应用,请你再举一例。
得分评卷人
四、实验探究(共17分)
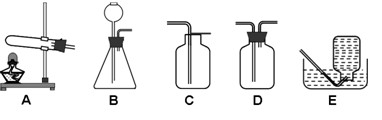
19.(9分)比较和归纳是学习化学的常用方法。某学习小组的同学在下图所列出的实验装置的基础上,对二氧化碳的制取进行研究。
(1)确定气体发生装置应考虑的因素是 ? 和 ? 。
(2)甲同学用大理石与稀盐酸反应制取二氧化碳气体,化学方程式是:
? ,要得到一瓶干燥的二氧化碳气体,所选装置的连接顺序是 ?(填字母),可选用 ? 作干燥剂。
(3)加热固体碳酸氢钠或固体碳酸氢铵都能产生二氧化碳气体,化学反应方程式分别是:2NaHCO3 Na2CO3+ H2O+ CO2↑; NH4HCO3 NH3↑+ H2O+ CO2↑
乙同学选择加热碳酸氢钠的反应制取二氧化碳,则发生装置应选用 ? (填字母)。他不选择加热碳酸氢铵制取二氧化碳的理由是 ? 。
20.(8分)某研究小组的同学为探究铁、铜、锌、银的金属活动性顺序,设计如图所示的三个实验(其中金属均已用砂纸打磨,且形状、大小相同;所用稀盐酸的溶质质量分数、用量也相同)。
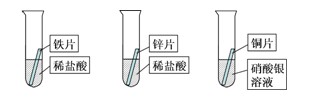
(1)通过观察,甲同学很快判断锌的活动性比铁强。据你分析,甲同学依据的实验现象是 。过一会儿,他又发现铜片表面有银白色固体附着,这说明 。
(2)乙同学认为上述实验不足以得出四种金属的活动性顺序,想再补充一个实验,请你和乙同学一起设计一个实验方案并进行实验,达到探究目的。
实验步骤实验现象实验结论
(3)通过以上探究,四种金属的活动性由强到弱的顺序是:
说明:
1.考生用其它方法做出正确答案的同样得分。
2.化学方程式中化学式(或元素符号)有错误不得分;未配平或未写反应条件扣1分;“↑” 或“↓”漏标两个以上扣1分。
一、选择(共28分,1—11题每题2分,12—13题每题3分。不选、多选、错选不得分)
题号12345678910111213
答案BDADBCCAABCDD
二、填空(共14分)
14.(4分)
(1)H2O(1分);(2)H2SO4(1分);(3)NaOH(1分);(4)Na2SO4(1分)
15.(6分)
(1)氮气的化学性质不活泼(2分);
(2)矿井内空气中混有甲烷,遇火容易爆炸(2分);
(3)这一部位的铁、氧气、水接触充分(2分)
16.(4分)2H2 + O2 2H2O(2分);53(1分);非金属(1分)
三、应用(共16分)
17.(10分)
(1)挥发(1分);醋酸能与铁反应(1分);
Fe + H2SO4= Fe SO4 + H2↑(其它合理答案均可得分)(2分);
(2)分别取少许白色固体,滴加食醋,有气泡产生的是纯碱,无现象的是食盐(2分);
(3)碱(1分);盐(1分); CaCO3↓+2NaOH(2分)
18.(6分)
(1)解:设至少需要熟石灰的质量为 污水中HCl的质量:
1000t×0.0073%=0.073t (1分)
2HCl + = CaCl2 + 2H2O (1分)
73 74
0.073t (1分)
(1分)
(1分)
答:(略)
(2)用熟石灰改良酸性土壤(1分)(其它合理答案均可得分)
四、实验探究(共17分)
19.(9分)
(1)反应物的状态(1分);反应的条件(1分);
(2)CaCO3 + 2HCl= CaCl2 + H2O + CO2↑(2分);B、D、C(2分);浓硫酸(1分);
(3)A(1分);反应生成二氧化碳的同时也生成氨气,使制得的气体不纯(1分)
20.(8分)
(1)锌与稀盐酸反应比铁剧烈(或锌片表面比铁片表面产生的气泡快)(1分);铜的活动性比银强(1分);
(2)
实验步骤实验现象实验结论
将用砂纸打磨过的铁片浸入硫酸铜溶液中,仔细观察。(2分)铁片表面有红色固体附着(2分)铁的活动性比铜强(1分)
(其它合理答案均可)
(3)锌铁铜银(1分)
| 语文试题 | 数学试题 | 英语试题 | 政治试题 | 物理试题 | 化学试题 | 历史试题 |
| 语文答案 | 数学答案 | 英语答案 | 物理答案 | 化学答案 | 历史答案 | 政治答案 |